
Նոր թեմա- Էլեկտրոլիտներ և ոչ էլեկտրոլիտներ։
Էլեկտրոլիտային դիսոցում
Հաղորդիչներ են այն նյութերը, որոնցում առկա են ազատ լիցքակիր մասնիկներ: Մետաղներում, որոնք համարվում են առաջին կարգի հաղորդիչներ, առկա են ազատ էլեկտրոններ, և էլեկտրական հոսանքը նրանցում էլեկտրոնների ուղղորդված հոսքն է.
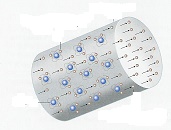
Որոշ նյութերի ջրային լուծույթներում (էլեկտրոլիտներում), որոնք համարվում են երկրորդ կարգի հաղորդիչներ, էլեկտրական հոսանքը իոնների հոսք է, այսինքն՝ էլեկտրոլիտներին բնորոշ է իոնային հաղորդականությունը.
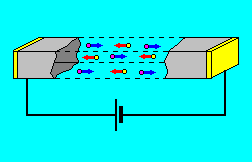
Դեռևս 1830-ական թվականներին անգլիացի ֆիզիկոս և քիմիկոս Մ. Ֆարադեյը նյութերը բաժանել է երկու խմբի՝ էլեկտրոլիտներ և ոչ էլեկտրոլիտներ:

Էլեկտրոլիտներ են այն նյութերը, որոնց ջրային լուծույթները էլեկտրական հոսանք են հաղորդում, իսկ ոչ էլեկտրոլիտներ են այն նյութերը, որոնց ջրային լուծույթները էլեկտրական հոսանք չեն հաղորդում:
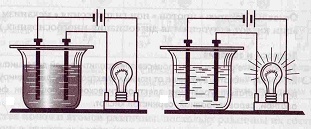
Նյութի պատկանելիությունը էլեկտրոլիտներին կարելի է ստուգել էլեկտրահաղորդականություն ստուգող սարքի միջոցով: Ինչպես երևում է նկարում, ոչ էլեկտրոլիտները հոսանք չեն անցկացնում, ինչի պատճառով լամպը չի վառվում, իսկ էլեկտրոլիտներում՝ վառվում է:
Աղերը, թթուները, հիմքերը էլեկտրոլիտ են, իսկ օրգանական միացությունների մեծ մասը (գլյուկոզ, սպիրտ, շաքար, ացետոն և այլն), ինչպես նաև մի շարք անօգանական նյութեր (թթվածին՝ O2, ազոտ՝ N2, ազոտի(I) օքսիդ՝ N2O և այլն) էլեկտրոլիտ չեն:
Հալված վիճակում հոսանքի հաղորդիչներ են նաև իոնական կապով բազմաթիվ միացություններ. աղեր, հիմքեր և որոշ օքսիդներ:
Գազային վիճակում գտնվող որոշ նյութերի (քլորաջրածին, բրոմաջրածին, ծծմբաջրածին և այլն) ջրային լուծույթները նույնպես էլեկտրական հոսանքի հաղորդիչներ են:
Իսկ ինչպե՞ս են ստեղծվում լիցքակիր մասնիկները՝ իոնները էլեկտրոլիտների լուծույթներում և հալույթներում: Առաջինն այս հարցին պատասխանել է շվեդ գիտնական Սվանտե Արենիուսը, ձևակերպելով էլեկտրոլիտային դիսոցման տեսության հիմնական դրույթները:
Էլեկտրոլիտները հալչելիս կամ ջրում լուծվելիս տրոհվում են իոնների. ենթարկվում են էլեկտրոլիտային դիսոցման.հալույթում տեղի է ունենում ջերմային դիսոցում.
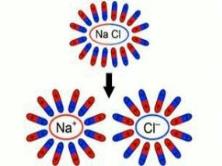
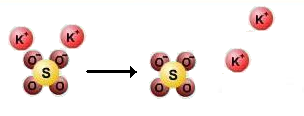
*Ջրային լուծույթներում իոնները քիմիապես կապված են ջրի մոլեկուլների հետ. հիդրատացված են, ինչի շնորհիվ տեղի է ունենում էլեկտրոլիտային դիսոցում.
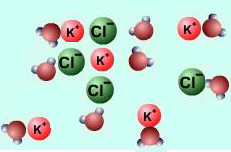
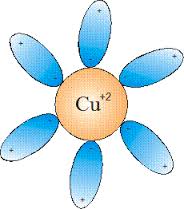
Սակայն դիսոցման հավասարումներ գրելիս իոնները հիդրատացված ձևով չեն ներկայացնում, այլ գրվում են պարզ ձևով.
օրինակ՝ KCl→K++Cl−CuSO4→Cu2++SO2−4
Նկատենք, դիսոցման հետևանքով ստացված իոնների թիվը (քանակը) միշտ ավելի մեծ է սկզբնական մոլեկուլների թվից (քանակից):
*Իոններն ատոմներից տարբերվում են ինչպես էլեկտրոնային կառուցվածքով, այնպես էլ հատկություններով:
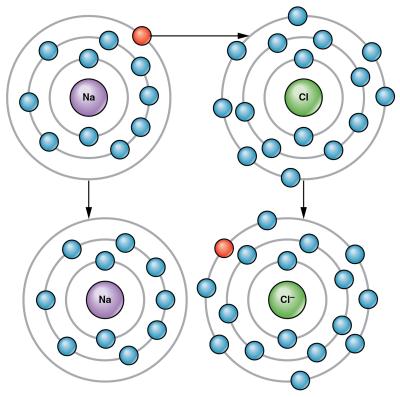
*Էլեկտրոլիտային դիսոցման գործընթացը դարձելի է. դիսոցման հետ միաժամանակ տեղի է ունենում ասոցում՝ իոններից մոլեկուլների առաջացում:
Օրինակ՝ HF⇄H++F−

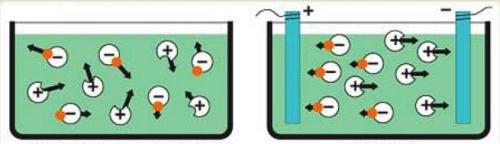
*Էլեկտրոլիտի լուծույթի կամ հալույթի միջով հաստատուն էլեկտրական հոսանք անցկացնելիս իոնների անկանոն շարժումը կարգավորվում է. դրական լիցքավորված իոնները՝ կատիոնները շարժվում են դեպի կաթոդ, իսկ բացասական լիցքավորված իոնները՝ անիոնները՝ դեպի անոդ:
Առաջադրանք
- Ըստ հաղորդականության`ինչպե՞ս են դասակարգվում ջրում լուծելի նյութերը:
Ըստ հաջորդականության ջրում լուծելի նյութերը բաժանվում են 2խմբի` էլեկտրոլիտներ և ոչ էլեկտրոլիտներ։
2. Ո՞ր նյութերն են էլեկտրոլիտները: Առաջարկե՛ք էլեկտրոլիտների հինգ օրինակ:
3. Ո՞ր նյութերն են ոչ էլեկտրոլիտները: Առաջարկե՛ք ոչ էլեկտրոլիտների երեք օրի- նակ:
Ոչ էլեկտրոլիտներն այն նյութերն են, որոնց ջրային լուծույթներն էլեկտրական հոսանք չեն հաղորդում, օրինակ ՝ օրգանական միացությունների մեծ մասը, ինչպես նաև ՝ մի շարք անօրգանական նյութեր ՝ թթվածինը (O2), ազոտը (N2), ազոտի (I) օքսիդը (N2O) և այլն:
4. Հետևյալ նյութերից երկու սյունակով դուրս գրեք համապատասխանաբար էլեկ- տրական հոսանքի հաղորդիչներն ու էլեկտրական հոսանքի ոչ հաղորդիչները (պինդ վիճակում).
պղինձ, փայտ, ալյումին, կալցիումի ֆտորիդ, բամբակ, երկաթ, մարմար, արծաթ, կալիումի բրոմիդ, նատրիումի հիդրօքսիդ:
Հաղորդիչներ-պղինձ, ալյումին, երկաթ, արծաթ։
Ոչ հաղորդիչներ-փայտ, կալցիումի ֆտորիդ, բամբակ, մարմար, կալիումի բրոմիդ, նատրիումի հիդրօքսիդ։
5)Հետևյալ նյութերից երկու սյունակով դո՛ւրս գրեք համապատասխանաբար ոչ էլեկտրոլիտներն ու էլեկտրոլիտները. քլորաջրածին, խաղողաշաքար, էթիլ սպիրտ, նատրիումի նիտրատ, ացետոն,ազոտական թթու, կալիումի քլորիդ, ավազ:
Էլեկտրոլիտ-քլորաջրածին, նատրիումի նիտրատ, ազոտական թթու, կալիումի քլորիդ։
Ոչ էլետրոլիտ-էթիլ սպիրտ, խաղողաշաքար ացետոն, ավազ։
